metabolit primer dan sekunder
- Dapatkan link
- X
- Aplikasi Lainnya
metabolit primer dan sekunder
Biosintesis merupakan proses pembentukan suatu metabolit (produk metabolisme)
dari molekul yang sederhana hingga menjadi molekul yang lebih kompleks yang
terjadi pada organism hidup (Neumann et al. 1985). Metabolisme pada makhluk
hidup dapat dibagi menjadi metabolisme primer dan sekunder. Metabolisme
primer menghasilkan metabolit primer sedangkan metabolism sekunder menghasilkan metabolit sekunder.
dari molekul yang sederhana hingga menjadi molekul yang lebih kompleks yang
terjadi pada organism hidup (Neumann et al. 1985). Metabolisme pada makhluk
hidup dapat dibagi menjadi metabolisme primer dan sekunder. Metabolisme
primer menghasilkan metabolit primer sedangkan metabolism sekunder menghasilkan metabolit sekunder.
Metabolisme primer padatumbuhan, seperti respirasidan fotosintesis, merupakan proses yang esensial bagi kehidupan tumbuhan. Tanpa adanya metabolisme primer, suatu organism akan terganggu pertumbuhan, perkembangan, serta reproduksinya, dan akhirnya mati. Berbeda dengan metabolisme sekunder, metabolism sekunder merupakan proses yang tidak esensial bagi kehidupan organisme. Tidak ada atau hilangnya metabolit sekunder tidak menyebabkan kematian secara langsung bagi tumbuhan, tapi dapat menyebabkan berkurangnya ketahanan hidup tumbuhan secara tidak langsung (misalnya dari serangan herbivore dan hama), ketahanan terhadap penyakit, estetika, atau bahkan tidak memberikan efek sama sekali bagi tumbuhan tersebut.
Pada fase pertumbuhan, tumbuhan utamanya memproduksi metabolit primer, sedangkan metabolit sekunder belum atau hanya sedikit di metabolisme. Sedangkan metabolism
sekunder terjadi pada saat sel dalam tahap diferensiasi menjadi sel yang
lebih terspesialisasi (fasestasioner) (Schripsema & Verpoorte 1994, Mohr & Schopfer 1995).
sekunder terjadi pada saat sel dalam tahap diferensiasi menjadi sel yang
lebih terspesialisasi (fasestasioner) (Schripsema & Verpoorte 1994, Mohr & Schopfer 1995).
Hasil metabolism dalam organism hidup dapat dibagi menjadi dua kelompok besar: metabolit primer dan sekunder. Yang tergolong dalam metabolit primer adalah senyawa-senyawa yang diproduksi dan terlibat pada jalur metabolisme primer (contohnya glikolisis, siklus asam sitrat/siklus Krebs, dan fotosintesis). Contoh metabolit primer adalah protein, karbohidrat, lipid, asam amino, nukleotida, danasetil CoA (Siegler 1998). Karbohidrat biasa disebut hidrat arang. Terdiri dari dua reaksi pembentukan dan pemecahan karbohidrat. Tersusun atas monomer molekul-molekul gula sederhana. Reaksi pemecahan terjadi di membrane sel yang melibatkan proses respirasi dan fermentasi. Reaksi pembentukan terjadi di dalam kloroplas yang melibatkan penggunaan karbondioksida untuk menghasilkan monomer gula sederhana (misal: sukrosa). Protein merupakan salah satu metabolit primer yang menyusun tubuh organisme. Menurut dogma biologi molekuler, DNA akan ditranskripsi menjadi RNA, RNA ditranslasi menjadi triplet kodon yang membentuk asam amino, polimer asam amino merupakan protein. Lipida merupakan salah satu metabolit promer hasil dari jalur oksidasi pentose fosfat. Reaksi pembentukan lipida terjadi di dalam sitosol tanaman. Lipida tersusun atas asam lemak dan gliserol pada umumnya. Asam nukleat merupakan metabolit primer yang menjadi dasar pembentuk materi genetic baik DNA/RNA dan juga turunannya dapat membentuk protein. Asam nukleat berperan dalam membentuk purin dan pirimidin.
Metabolit sekunder tanaman merupakan senyawa dengan berat molekul rendah yang diproduksi tanaman sebagai respon terhadap ancaman lingkungan dan patogen. Hasil studi menunjukkan bahwa produk metabolit sekunder merupakan senyawa yang diturunkan dari metabolit primer, yaitu karbohidrat, protein, lipid, dan asam nukleat. Secara sederhana, metabolit sekunder tanaman terbagi atas tiga golongan besar, yaitu fenolik, senyawa bernitrogen, dan terpenoid (Edwards & Gatehouse 1999).
Metabolit sekunder tidak digunakan untuk proses pertumbuhan dan unik untuk setiap organisme. Pada umumnya senyawa metabolit sekunder berfungsi sebagai mekanisme pertahanan diri, misalnya sebagai pelindung (protectant) dari gangguan hama untuk tumbuhan itu sendiri atau lingkungannya. Selain sebagai pelindung, dapat juga berfungsi sebagai penarik (attractan) atau penolak (repellant) dari serangga atau herbivora. Contoh metabolit sekunder lainnya pada tumbuhan adalah pigmen-pigmen, senyawa antibiotik, senyawa bioaktif, dan senyawaaromatik (Siegler 1998).
Produksi senyawa metabolit primer maupun sekunder saat ini sangat penting, misalnya dalam bidang industri, kesehatan, atau pangan. Sebagai contoh, saat ini senyawa metabolit sekunder telah banyak digunakan sebagai zat warna, racun, aroma makanan, obat-obatan, dan sebagainya. Dengan mempelajari jalur biosintesis ini memungkinkan untuk melakukan modifikasi dari jalur tersebut sehingga dapat diproduksi metabolit dalam jumlah yang lebih banyak dalam waktu yang lebih singkat, mengetahui struktur metabolit yang dihasilkan, dan dapat dilakukan sintesis untuk menghasilkan derivatnya (Lisdawati et al. 2007).
Biosintesis Metabolit sekunder
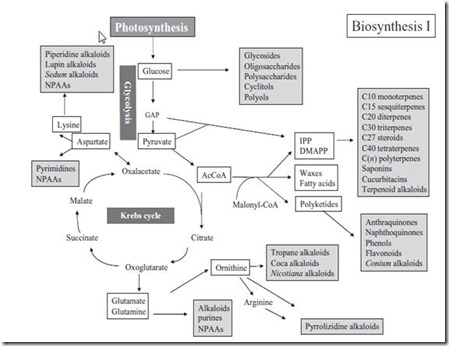
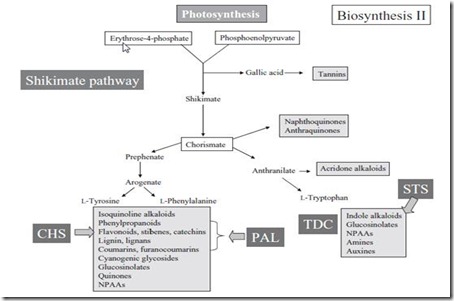
Ada 2 lintasan biosintesis MS. Pertama adalah lintasan metabolisme dasar seperti glikolisis dan siklus Krebs. Kedua adalah lintasan shikimate. Lintasan metabolisme dasar dan shikimate (Wink, 2010) masing-masing dapat dilihat pada Gambar 1 dan Gambar 2.
Gambar 1. Lintasan metabolisme dasar dari sintesis metabolit sekunder (Wink, 2010)
Gambar 2. Lintasan shikimate sintesis metabolit sekunder (Wink, 2010)
Poliamina
Poliamina adalah senyawa polikation berberat molekul rendah yang ditemukan dalam semua makhluk hidup (Kaur-Sawhney, 2003; Kusano, 2008), seperti bakteri, jamur, hewan, dan tanaman tingkat tinggi (Baron dan Stasolla (2008). Dilihat dari strukturnya, poliamina termasuk dalam golongan amina. Namun, secara fisiologis, poliamina bisa dimasukkan ke dalam golongan alkaloid (Harbone, 1984; Robert, 2010).
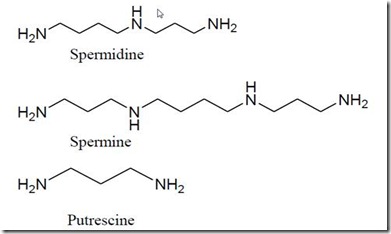
Secara kimiawi, poliamina merupakan senyawa organik yang mempunyai dua atau lebih gugus amino utama –NH2, dapat berupa senyawa sintetik dan juga alami. Senyawa poliamina sintetik termasuk etilen diamine H2N–CH2–CH2–NH2, 1,3-diaminopropane H2N–(CH2)3–NH2, dan hexamethylenediamine H2N–(CH2)6–NH2. Senyawa poliamina alami meliputi putrescine H2N–(CH2)4–NH2, cadaverine H2N–(CH2)5–NH2, spermidine H2N–(CH2)4–NH–(CH2)3–NH2, and spermine H2N–(CH2)3–NH–(CH2)4–NH–(CH2)3–NH2n (Wikipedia, 2012). Struktur molekul poliamina alami dapat dilihat pada Gambar 3.
Gambar 3. Molekul Poliamina (sumber: Oryza, 2012)
Pada sel tumbuhan poliamina terdapat terutama dalam bentuk diamine putrescine (Put), triamine spermidine (Spd), dan tetramine spermine (Spm)( Kaur-Sawhney (2003; Vadim, 2009). Poliamina ini ada dalam bentuk bebas atau sebagai konjugat yang terikat pada asam fenolik dan pada senyawa berberat molekul rendah lain atau pada makromolekul seperti protein dan asam nukleat (Kaur-Sawhney, 2003)
Groppa dan Benavides (2007) menyatakan bahwa Put, SPd, dan Spm merupakan Poliamina utama yang dijumpai pada semua sel makhluk hidup. Senyawa ini merupakan senyawa nitrogen alifatik yang bermuatan positif pada pH fisiologis. Sifatnya ini memungkinkan poliamina berinteraksi dengan makromolekul yang bermuatan negatif, seperti DNA dan RNA, protein dan fosfolipid.
Menurut Kusano (2008) awal penemuan poliamina adalah sekitar tahun 1678 ketika ditemukan kristal tiga sisi pada semen manusia. Karena banyak terdapat dalam sperma, maka senyawa ini dinamai dengan spermine. Spermidine pertama ditemukan pada pankreas. Spermine dan spermidine bertanggung jawab pada bau khas dari semen. Dua senyawa lainnya putrescine dan cadaverine ditemukan pada bakteri dekomposisi.
Biosintesis Poliamina
Pada tanaman, poliamina terdapat dalam sitoplasma, vakuola, mitokondria dan kloroplas. Sintesis poliamina dimulai dari dua molekul prekursor asam amino, yaitu L-arginine dan L-methionine (Kusano, 2008).
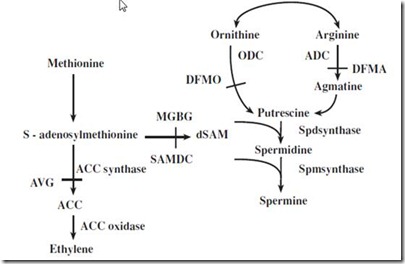
Ada dua lintasan alternatif. Lintasan pertama, dimulai dari arginine. Kemudian, diamine putrescine disintesis melalui ornithine oleh arginase dan ornithine dekarboksilase. Putrescine dapat juga disintesis melalui agmatine oleh tiga reaksi berantai yang dikatalisir masing-masing oleh enzim arginine dekarboksilase, agmatine iminohydrolase, dan N-carbamoylputrecine amidohydrolase. Putrescine dikonversi menjadi spermidine oleh aksi spermidine sintase. Lintasa kedua, dimulai dari methionin kemudian diubah menjadi S-adenosylmethionine dua reaksi yang berurutan oleh methionine adenosyltransferase dan S-adenosylmethionine dekarboksilase (Kusano, 2008)
Secara ringkas, poliamina disintesis dari arginine dan ornithine oleh arginine decarboxylase dan orthinine decarboxylase. Senyawa antara agmatine, yang disintesis dari arginine, diubah menjadi Put, yang kemudian ditransformasi menjadi Spd dan Spm . Untuk lebih jelasnya, lintasan biosintesis Poliamina dapat dilihat pada Gambar 4 (Kaur-Sawhney, 2003). Biosisntesis alternative, methionin diubah menjadi S-adenosylmethionine oleh methionine adenosyltransferase dan S-adenosylmethionine dekarboksilase kemudian terbentuk spermidine dan berikutnya spermine (Kusano, 2008). Lintasan biosintesis poliamina dapat dilihat pada Gambar 4.
Gambar 4. Lintasan biosintesis poliamina pada tumbuhan (Kaur-Sawhney, 2003).
Peran dan Kegunaan Poliamina
Dari beberapa macam pendekatan dan bukti yang ada, poliamina terlibat dalam banyak proses di dalam tanaman. Proses tersebut berupa 1) proses fisiologis pertumbuhan dan perkembangan dan 2) proses pertahanan dan kelangsungan hidup.
Pada proses pertumbuhan dan perkembangan, poliamina terlibat dalam beragam proses seperti replikasi DNA, transkripsi gen, pembelahan sel, perkembangan organ, perkembangan dan pemasakan buah, senescence daun (Kaur-Sawhney, 2002; Groppa dan Benavides, 2007; Kusano, 2008; Gilli dan Tusteja , 2010). Baron dan Stasolla (2008) memberikan daftar yang lebih panjang lagi terhadap keterlibatan poliamina dalam proses fisiologis tumbuhan. Proses tersebut meliputi pembelahan sel, embriogenesis, organogenesis, perkembangan bintil akar, perkembangan bunga, buah, dan polen, senescence, perkecambahan benih, sintesis alkaloid tropane, dinamisasi sitoskeletal, respons stres, fotosintesis, dan berinteraksi dengan hormon. Kusano (2008) menambah daftar peran poliamina, termasuk regulasi ekspresi gen, translasi, proliferasi sel, modulasi signaling sel, dan stabilisasi membran. Poliamina juga memodulasi aktivitas unit tertentu dari saluran ion.
Poliamina juga terlibat dalam proses pertahanan dan kelangsungan hidup. Peran poliamina ini terlihat pada tumbuhan yang mengalami cekaman, baik cekaman abiotik maupun cekaman biotik ((Kaur-Sawhney, 2002; Groppa dan Benavides, 2007; Kusano, 2008; Gilli dan Tusteja , 2010). Pada cekaman abiotik, seperti salinitas, kekeringan, suhu ekstrem, hipoksia, dan malnutrisi, tanaman banyak mengakumulasi poliamina. Pada cekaman biotik, seperti serangan hama dan penyakit, tanaman juga meresponsnya dengan meningkatkan konsentrasi poliamina dalam sel pada jaringan yang terserang (Baron dan Stasolla (2008) ); Kusano, 2007).
Dari segi manfaatnya, poliamina dapat digunakan untuk penanda kanker dan penemuan obat anti kanker. Menurut Vadim (2009) poliamina terlibat dalam sejumlah reaksi biokimia dan digunakan sebagai penanda kanker dan analognya digunakan sebagai obat anti kanker.
Dalam dunia farmasi dan kecantikan, poliamina diklaim dapat memberberikan banyak manfaat. Oryza (2011) menyebutkan bahwa poliamina dapat mencegah arteriosceloris, merangsang pertumbuhan rambut dan kuku, merangsang keratinocytes dan keratin serta berperan sebagai anti aging.
Peran Poliamina terhadap Cekaman Abiotik
Palavan-Ünsal (1995) menyatakan bahwa tanaman tingkat tinggi yang terpapar kondisi lingkungan yang suboptimal atau tercekam meresponsnya dengan mengakumulasi Putrescin dalam konsentrasi tinggi. Pengamatan ini awalnya dimulai oleh Richards dan Coleman tahun 1952 pada tanaman barley yang ditanam pada kultur hidroponik yang kekurangan ion K+. Sejak itu, kondisi cekaman lain juga menunjukkan akumulasi putrescin, antara lain kekurangan air, konsentrasi osmotik internal dan eksternal yang tinggi, konsentrasi NH4+ yang tinggi, H+ dan konsentrasi kation monovalen lainnya, larutan ambien, polutan SO2, O3, Pb2+, suhu rendah, dan suhu tinggi.
Groppa dan Benavides (2008) mereview peran poliamina terhadap salinitas, kekeringan dan stres osmotik. Mereka menyatakan bahwa cekaman garam dan kekeringan adalah dua cekaman abiotik utama di bidang pertanian dan rendahnya potensi air merupakan konsekuensi umum dari keduanya. Salinitas merupakan kendala lingkungan yang kompleks yang disebabkan oleh dua hal, yakni 1) komponen osmotik karena penurunan potensi osmotik eksternal dari larutan tanah dan 2) komponen ionik yang terkait dengan akumulasi ion beracun pada konsentrasi tinggi (terutama Na dan Cl). Konsentrasi garam yang tinggi mengganggu integritas membran sel, aktivitas berbagai enzim dan fungsi aparatus fotosintesis.
Tanaman menanggapi perubahan kondisi lingkungan yang kurang menguntungkan ini dengan mengakumulasi senyawa osmolit berberat molekul rendah seperti prolin dan poliamina. Sampai saat ini, masih belum jelas komponen stres garam yang mana yang bertanggung jawab terhadap akumulasi poliamina, apakah komponen osmotik ataupun komponen ionik, meski banyak laporan telah mencoba untuk menjelaskan petunjuk penting ini selama bertahun-tahun. Demikian pula, belum jelas benar poliamina yang mana yang paling berperan pada kondisi stres ? apakah putrescin, spermidin, atau spermin.
Pengukuran kandungan poliamina pada beberapa kultivar padi menunjukkan bahwa kultivar padi yang toleran garam mempertahankan taraf poliamina yang tinggi, yaitu spermidin (Spd) dan spermin (Spm), sedangkan kultivar padi sensitif garam hanya mempertahankan putrescin (Put) yang tinggi. Kultivar toleran garam AU1, Co43, dan CSC1 efektif dalam mempertahankan konsentrasi Spd dan Spm yang tinggi, sedangkan kandungan Putrescin tidak signifikan berubah pada analisis pertumbuhan ketika tanaman terpapar salinitas.
Sensitivitas terhadap garam pada padi dikaitkan dengan tingginya akumulasi putrescin dan rendahnya Spd dan Spm dalam tunas kultivar sensitif garam Co36 CSC2, GR3, IR20, TKM4, dan TKM9 pada kondisi salin. Membran plasma akar kultivar padi toleran garam Nonabokra dan Pokkali kaya akan Spm dan Spd, sedangkan membran plasma akar kultivar sensitif (M-1-48 dan IR8) hanya kaya akan Put.
Kelihatannya Spd dan Spm berperan terhadap komponen osmotik dan responsnya lebih lama sedangkan Put lebih berperan terhadap komponen ionik yang beracun dan responsnya lebih cepat tetapi sementara. Pada penelitian menggunakan NaCl (100 dan 200 mM) dan mannitol (200 dan 400 mM) pada kalus Fraxinus angustifolia, ditemukan bahwa dalam waktu singkat (30 menit) Put dan Spd meningkat sebagai konsekuensi dari perlakuan garam, dan akumulasi yang terus berlanjut dari Spd dan Spm akibat mannitol.
Poliamina kemungkinan besar berperan dalam menambah rigiditas permukaan membran mikrosomal, menstabilkannya terhadap NaCl dan stres osmotik. Lebih lanjut, konsentrasi poliamina yang lebih tinggi yang terikat pada membran mikrosomal kemungkinan dapat mengurangi pengaruh buruk dari NaCl dan kekurangan air.
Dalam kaitannya dengan kekeringan, kelihatannya spermidin lebih berperan, diikuti spermin. Ada penelitian yang melaporkan bahwa Spd merupakan poliamina utama dalam jaringan yang tercekam kekeringan. Penelitian pada akar kecambah chickpea dan kedelai berumur 7 hari yang diperlakukan dengan cekaman kekeringan 0,8 MPa, menunjukkan bahwa total dan individu poliamina lebih tinggi pada chickpea dibanding kedelai. Tanaman chickpea lebih tahan kekeringan dan mengandung lebih banyak Put dan Spd dibanding tanaman kedelai. Kecambah barley yang diperlakukan dengan Spd sebelum periode kekurangan air mampu mengembalikan peningkatan aktivitas enzim katalase dan peroksidase guaiaco, yang mengindikasikan bahwa Spd dapat mempengaruhi aktivitas enzim penangkap H2O2, dan memoderatkan taraf molekul isyarat ini. Tanaman padi merespons kekeringan dengan meningkatkan Put endogen, tetapi tidak cukup tinggi untuk dikonversi menjadi Spd dan Spm. Sebaliknya, tanaman padi transgenik (Datura adc) menghasilkan Put yang lebih tinggi pada cekaman kekeringan sehingga memacu sintesis Spd dan Spm, kemudian melindungi tanaman dari cekaman kekeringan.
Kusano et al. (2008) lebih jauh mengelaborasi peran poliamina terhadap stres abiotik, khususnya kekeringan. Pada tanaman Arabidopsis, mutan acl5/spms, yang tak mampu memproduksi spermin, menunjukkan hipersensitif terhadap stres garam dan kekeringan dibanding tanaman normal. Fenotipe stres sensitif ini dapat pulih dengan penambahan poliamina eksogen, yaitu putrescin untuk sensitif garam dan spermin untuk sensitif kekeringan. Tanaman Arabidopsis mutan acl5/spsm ini juga hipersensitif terhadap KCl dan tanaman ini juga kekurangan Ca2+. Dari fenomena ini, dapat disimpulkan bahwa kekurangan spermin dapat menyebabkan ketidakteraturan keluar-masuknya ion Ca2+, yang mengakibatkan berkurangnya daya adaptasi terhadap tingginya NaCl dan stres kekeringan. Konsisten dengan data yang ada, poliamina, termasuk spermin, juga dilaporkan menghambat pembukaan stomata dan menginduksi penutupannya. Baru-baru ini juga dilaporkan bahwa poliamina mencegah aliran K+.
Gill dan Tuteja (2010) mengelaborasi aplikasi poliamina eksogen terhadap cekaman kekeringan. Banyak bukti mengindikasikan bahwa aplikasi poliamina eksogen dapat menstabilkan membran sel tanaman dan melindunginya dari kerusakan akibat kondisi stres. Poliamina juga diindikasikan ikut berperan dalam menjaga integritas membran. Pemberian Putrescin eksogen terbukti dapat mengurangi kerusakan oksidatif akibat genangan air pada Allium fistulosuma dengan meningkatnya kapasitas antioksidan. Ditemukan juga bahwa aplikasi Put eksogen menyebabkan berkurangnya kandungan senyawa radikal superoksida O2 dan H202, sehingga mengurangi stres oksidatif pada sel tanaman.
Produksi Poliamina
Konsentrasi poliamina dalam sel normal tumbuhan ada pada rentang dari beberapa ratus mikromolar sampai beberapa milimolar. Konsentrasi ini diatur secara ketat, karena pada taraf yang lebih tinggi, poliamina bersifat racun terhadap sel dan bisa menyebabkan kematian sel (Kusano, 2008). Kekecualian ada pada sel kanker. Pada sel kanker, konsentrasi poliamina melebihi konsentrasi pada sel normal (Yatin, 2002). Pengaturan konsentrasi poliamina dalam sel kelihatannya dilakukan tanaman pada beberapa tahapan proses produksi poliamina.
Produksi Poliamina dalam tumbuhan ditentukan oleh empat hal, yaitu sintesis, penyerapan, transpor, dan degradasi (Yatin, 2002;Kusano, 2008). Namun demikian, penyerapan dan transpor poliamina belum dapat dipertimbangkan dalam proses produksi karena kedua proses tersebut belum diketahui secara detail. Kusano (2008) menyatakan bahwa transpor poliamina pada tumbuhan masih dalam bentuk hipotesis. Demikian pula halnya, poliamina degradasi, mekanismenya masih belum cukup jelas. Untuk poliamina penyerapan, Yatim (2002) menyatakan bahwa poliamina penyerapan dan poliamina sintesis dapat saling disubstitusi. Oleh karena itu, untuk saat ini, pertimbangan bagi produksi poliamina hanyalah dari sisi sintesisnya.
Pada tahap sintesis, produksi poliamina kemungkinan dapat dimanipulasi dengan berbagai cara antara lain dengan memanipulasi bahan baku, produk antara, enzim-enzim yang terlibat, dan faktor lingkungan yang mempengaruhi produksi poliamina dalam lintasannya, terutama faktor cekaman biotik dan abiotik. Namun demikian, pemilihan bahan baku dan paparan terhadap cekaman merupakan pendekatan yang lebih praktis.
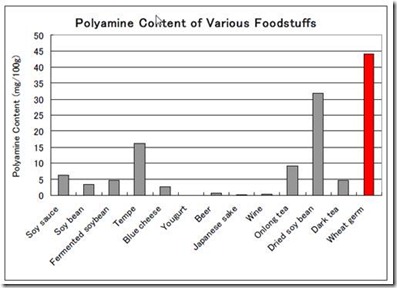
Beberapa jenis tanaman secara alamiah mengandung banyak poliamina di dalam sel dan jaringannya. Menurut Okamoto (1997) dan Oryza (2011) gandum, kedelai dan turunannya, serta teh mengandung banyak poliamina. Kandungan poliamina pada berbagai jenis bahan pangan yang berasal dari tumbuhan disajikan pada Gambar 5.
Paparan tumbuhan pada berbagai cekaman juga merupakan pilihan yang rasional. Banyak penelitian telah membenarkan bahwa cekaman biotik dan abiotik meningkatkan kandungan poliamina dalam tumbuhan. Bentuk cekaman dapat berupa salinitas, kekeringan, suhu ekstrem, hipoksia, dan malnutrisi, serta serangan hama dan penyakit (Alcazar, 2006; Kusano, 2007). Namun demikian Selmar (2007) mengingatkan bahwa peningkatan kandungan metabolit sekunder, termasuk poliamina lebih bersifat kualitatif daripada kuantitatif. Hal ini dikarenakan umumnya tanaman dalam keadaan tercekam pertumbuhan dan produksi total biomassanya rendah, sehingga secara kuantitatif trade off dengan tingginya kandungan metabolit sekunder.
Gambar 5. Kandungan Poliamina dalam jenis pangan dan minuman (Oryza 2011).
permasalahan:
1. bagaimana metabolism sekunder terjadi pada saat sel dalam tahap diferensiasi menjadi sel yang lebih terspesialisasi?
2. Karbohidrat biasa disebut hidrat arang. Terdiri dari dua reaksi pembentukan dan pemecahan karbohidrat. apa saja kedua reaksi tersebut dan jelaskan?
3. Mengapa metabolit sekunder tidak digunakan untuk proses pertumbuhan dan unik untuk setiap organisme?
- Dapatkan link
- X
- Aplikasi Lainnya
Saya akan mencoba menjawab permasalahan tiga. Karena metabolit sekunder tidak selalu dihasilkan, tetapi hanya pada saat dibutuhkan saja atau pada fase-fase tertentu.Fungsi metabolit sekunder adalah untuk mempertahankan diri darikondisi lingkungan yang kurang menguntungkan, misalnya untuk mengatasi hama dan penyakit, menarik polinator,dan sebagai molekul sinyal. Singkatnya, metabolit sekunder digunakan organisme untuk berinteraksi dengan lingkungannya.
BalasHapussaya akan mencoba menjawab permasalahan yang kedua
BalasHapusKarbohidrat juga berperan penting dalam menentukan karakteristik bahan makanan, misalnya warna, rasa, tekstur dan lain-lain. Sedangkan dalam tubuh karbohidrat berguna untuk mencegah timbulnya ketosis, pemecahan protein yang berlebihan, kehilangan mineral dan berguna untuk metabolisme lemak dan protein (Winarno, 2002)
Pada tanaman, karbohidrat dibentuk dari reaksi karbohidrat dan air dengan bantuan klorofil dan sinar matahari pada jasad hidup autrotopik. Melalui proses fotosintesis ini kemudian mengalami polimerisasi menjadi pati atau selulosa.Secara kimia reaksi yang terjadi adalah sebagai berikut:
CO2 + H2O ® (CH2O)n + O2.
Saya akan menjawab permasalahan yang nomor 3. Metabolit sekunder adalah senyawa metabolit yang tidak esensial bagi pertumbuhan organisme. Oleh karena itu metabolit sekunder tidak berperan penting dalam proses pertumbuhan tumbuhan. Namun metabolit sekunder banyak di manfaatkan oleh tumbuhan untuk pertahanan diri, dll.
BalasHapussaya aakan mencoba menjawab no 3
BalasHapusMetabolit sekunder adalah senyawa metabolit yang tidak esensial bagi pertumbuhan organisme dan ditemukan dalam bentuk yang unik atau berbeda-beda antara spesies yang satu dan lainnya. Setiap organisme biasanya menghasilkan senyawa metabolit sekunder yang berbeda-beda, bahkan mungkin satu jenis senyawa metabolit sekunder hanya ditemukan pada satu spesies dalam suatu kingdom. Senyawa ini juga tidak selalu dihasilkan, tetapi hanya pada saat dibutuhkan saja atau pada fase-fase tertentu. Fungsi metabolit sekunder adalah untuk mempertahankan diri dari kondisi lingkungan yang kurang menguntungkan, misalnya untuk mengatasi hama dan penyakit, menarik polinator, dan sebagai molekul sinyal. Singkatnya, metabolit sekunder digunakan organisme untuk berinteraksi dengan lingkungannya.
Metabolisme sekunder (juga disebut metabolisme khusus) adalah istilah untuk jalur dan molekul kecil produk dari metabolisme yang tidak mutlak diperlukan untuk kelangsungan hidup organisme. Senyawa kimia sebagai hasil metabolit sekunder telah banyak digunakan untuk zat warna, racun, aroma makanan, obat-obatan dan sebagainya. Serta banyak jenis tumbuhan yang digunakan sebagai obat-obatan, dikenal sebagai obat tradisional sehingga perlu dilakukan penelitian tentang penggunaan tumbuh-tumbuhan berkhasiat dan mengetahui senyawa kimia yang bermanfaat sebagai obat.
Saya akan mencoba menjawab permasalahan Anda yang kedua:
BalasHapusUntuk reaksi pembentukan (glukoneogenesis), yaitu mengubah piruvat menjadi fosfoenolpiruvat (PEP), jadi membalik reaksi yang dikatalisis oleh piruvat kinase. Perubahan ini dilakukan dalam 4 langkah:
1. Piruvat mitokondria mengalami dekarboksilasi membentuk oksaloasetat. Reaksi ini memerlukan ATP (adenosin trifosfat) dan dikatalisis oleh piruvat karboksilase. Seperti banyak enzim lainnya yang melakukan reaksi fiksasi CO2, pada reaksi ini memerlukan biotin untuk aktivitasnya.
2. Oksaloasetat direduksi menjadi malat oleh malat dehidrogenase mitokondria. Pada reaksi ini, glukoneogenesis secara singkat mengalami overlap (tumpang tindih) dengan siklus asam sitrat.
3. Malat meninggalkan mitokondria dan dalam sitoplasma dioksidasi membentuk kembali oksaloasetat. Kemudian oksaloasetat sitoplasma mengalami dekarboksilasi membentuk PEP pada reaksi yang tidak memerlukan GTP (guanosin trifosfat) yang dikatalisis oleh PEP karboksikinase.
4. Reaksi pengganti kedua dan ketiga dikatalisis oleh fosfatase. Fruktosa-1,6-bisfosfatase mengubah fruktosa-1,6-bisfosfat menjadi fruktosa-6-fosfat, jadi membalik reaksi yang dikatalisis oleh fosfofruktokinase. Glukosa-6-fosfatase yang ditemukan pada permulaan metabolisme glikogen, mengkatalisis reaksi terakhir glukoneogenesis dan mengubah glukosa-6-fosfat menjadi glukosa bebas.
Sedangkan untuk reaksi pemecahan (glikolisis), yaitu engubahan molekul sumber energi, yaitu glukosa yang mempunyai 6 atom C manjadi senyawa yang lebih sederhana, yaitu asam piruvat yang mempunyai 3 atom C. Reaksi ini berlangsung di dalam sitosol (sitoplasma).
Pertama-tama, glukosa mendapat tambahan satu gugus fosfat dari satu molekul ATP, yang kemudian berubah menjadi ADP, membentuk glukosa 6-fosfat. Setelah itu, glukosa 6-fosfat diubah oleh enzim menjadi isomernya, yaitu fruktosa 6-fosfat. Satu molekul ATP yang lain memberikan satu gugus fosfatnya kepada fruktosa 6-fosfat, yang membuat ATP tersebut menjadi ADP dan fruktosa 6-fosfat menjadi fruktosa 1,6-difosfat. Kemudian, fruktosa 1,6-difosfat dipecah menjadi dua senyawa yang saling isomer satu sama lain, yaitu dihidroksi aseton fosfat dan PGAL (fosfogliseraldehid atau gliseraldehid 3-fosfat). Tahapan-tahapan reaksi diatas itulah yang disebut dengan fase investasi energi.
Selanjutnya, dihidroksi aseton fosfat dan PGAL masing-masing mengalami oksidasi dan mereduksi NAD+, sehingga terbentuk NADH, dan mengalami penambahan molekul fosfat anorganik (Pi) sehingga terbentuk 1,3-difosfogliserat. Kemudian masing-masing 1,3-difosfogliserat melepaskan satu gugus fosfatnya dan berubah menjadi 3-fosfogliserat, dimana gugus fosfat yang dilepas oleh masing-masing 1,3-difosfogliserat dipindahkan ke dua molekul ADP dan membentuk dua molekul ATP. Setelah itu, 3-fosfogliserat mengalami isomerisasi menjadi 2-fosfogliserat. Setelah menjadi 2-fosfogliserat, sebuah molekul air dari masing-masing 2-fosfogliserat dipisahkan, menghasilkan fosfoenolpiruvat. Terakhir, masing-masing fosfoenolpiruvat melepaskan gugus fosfat terakhirnya, yang kemudian diterima oleh dua molekul ADP untuk membentuk ATP, dan berubah menjadi asam piruvat.
Setiap pemecahan 1 molekul glukosa pada reaksi glikolisis akan menghasilkan produk kotor berupa 2 molekul asam piruvat, 2 molekul NADH, 4 molekul ATP, dan 2 molekul air. Akan tetapi, pada awal reaksi ini telah digunakan 2 molekul ATP, sehingga hasil bersih reaksi ini adalah 2 molekul asam piruvat (C3H4O3), 2 molekul NADH, 2 molekul ATP, dan 2 molekul air. Perlu dicatat, pencantuman air sebagai hasil glikolisis bersifat opsional, karena ada sumber lain yang tidak mencantumkan air sebagai hasil glikolisis.